B-breve M16V
Hvorfor valget af B. breve M-16V til modermælkserstatning?
Bifidobakterier udgør den absolut største andel af bakterier i tarmen hos et sundt, ammet spædbarn. Forskellige stammer producerer metabolitter, såsom kortkædede fedtsyrer i forskellige volumener og kommunikerer derfor forskelligt med f.eks. spædbarnets immunsystem.1,2 Og hvad betyder det så? Immunforsvaret støttes forskelligt af de forskellige, naturligt forekommende bakterier afhængigt af stammetype og mængden af disse. Derfor arbejder vi med bifidobakterier.
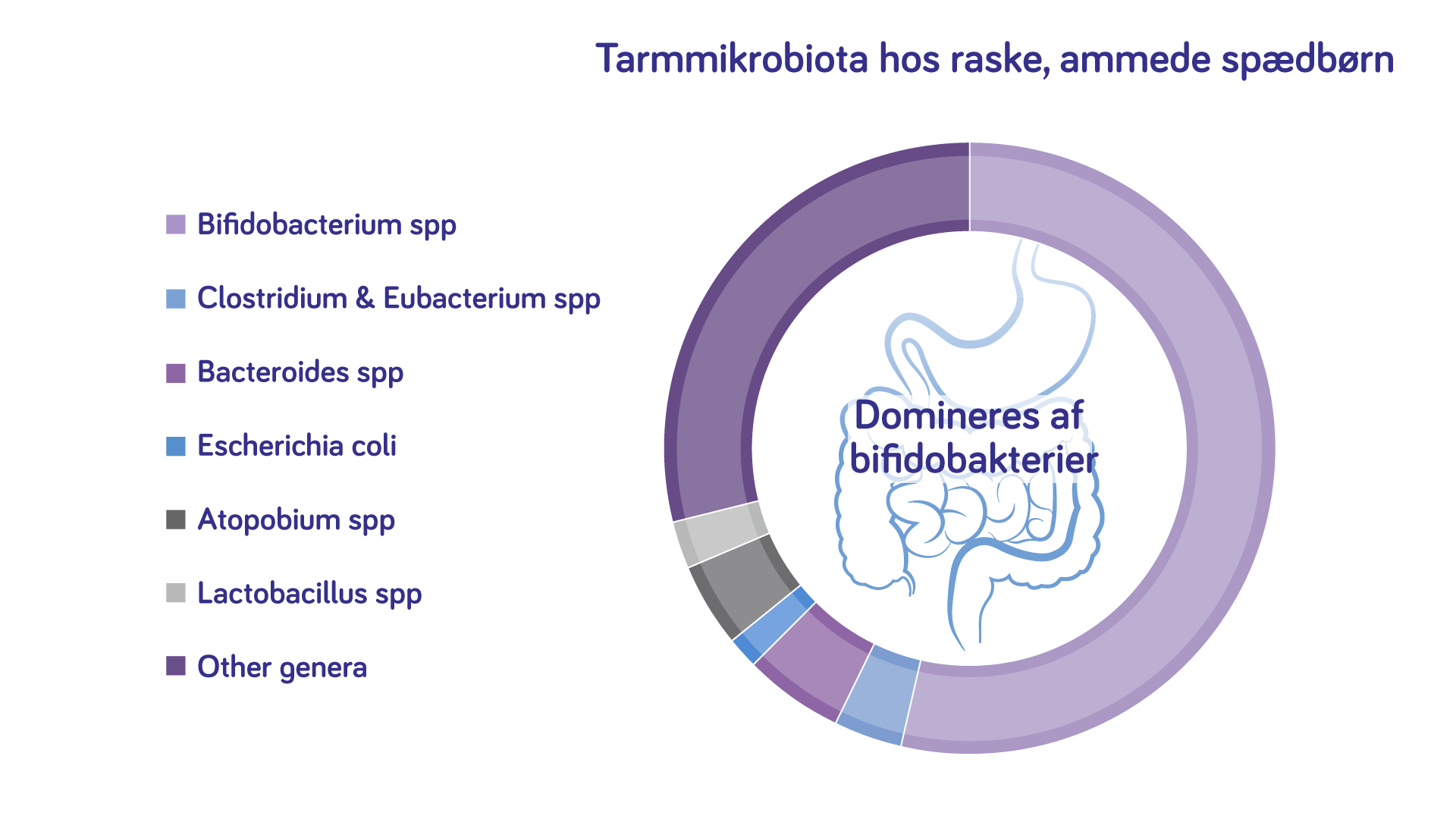
Figur 1: Udviklet af Nutricia.3,4,5
Metode for udvælgelse af B.breve
B.breve-bakterierne er de mest almindeligt forekommende bifidobakterier i brystmælk6, og B.breve og B.longum er de mest almindelige bifidobakterier i tarmmikrobiotaen hos ammede spædbørn.7
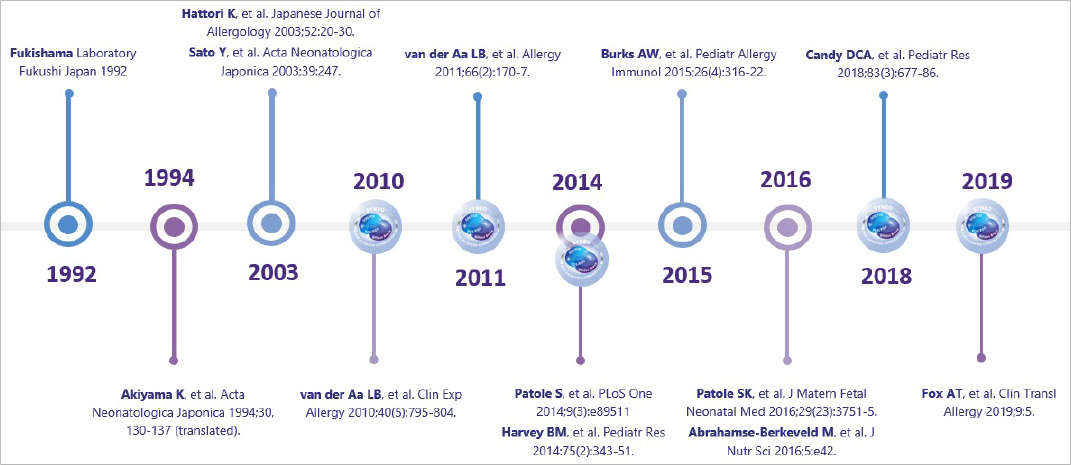
B.breve M-16V blev udvalgt blandt 400 forskellige stammer og er understøttet af 17 kliniske studier siden 1994. Dette er således ikke en ny eller ukendt bifidobakterie. B.breve M-16V er ligeledes undersøgt i forskellige populationer med allergi.
Faktisk er det klinisk bevist, at Bifidobacterium breve M-16V:
- Reducerer allergiske symptomer hos spædbørn med IgE-medieret atopisk dermatitis8
- Forbedrer ble-dermatitis og blødgør afføring9
- Forbedrer gastrointestinal udvikling10
- Forebygger astmalignende symptomer11
Præklinisk forskning har vist, at Bifidobacterium breve M-16V er den mest lovende stamme til at reducere allergiske symptomer og den har vist sig at have antiallergiske egenskaber.12
In Vitro
- Absence of pathogenicity
- No harmful substances or metabolites
- Devoid of virulence factors
- No mutagenicity
In Vivo
- Lack of toxicity (acute, chronic)
- No pathogenicity
- Reduced allergic symptoms (skin, respiratory)
Clinical Trials
- 5 completed trials (Morinaga): VLBW, preterm, term, CMA infants
- 5 completed trials (Nutricia): healthy infants, CMA infants, children, asthmatic adults (CT131, CT141, SYNBAD, MIPS, SMILE, ATOS, SYAS)
- 4 trials in progress (Nutricia): IgE-med. CMA (PRESTO), non-IgE med. CMA (ASSIGN), C-section babies (JULIUS), healthy infants (COLOR)
bläddra på mobil
- Davis EC, et al. Gut Microbes 2017;8(2):143–171.
- Davis EC, et al. Dig Dis Sci 2020; 65(3): 706–722.
- Davis EC, et al. Gut Microbes 2017;8(2):143–171.
- Davis EC, et al. Dig Dis Sci 2020; 65(3): 706–722.
- Lewis ZT, Nestlé Nutri Workshop Ser, 2017;88:149-59.
- Martin R, et al. Appl Env Microbiol. 2009;75:965–969.
- Davis EC, et al. Gut Microbes 2017; 8(2): 143–171.
- van der Aa LB, et al. Clin Exp Allergy 2010;40(5):795-804.
- van der Aa LB, et al. Clin Exp Allergy 2010;40(5):795-804.
- Wong CB et al. Nutrients. 2019 Aug; 11(8): 1724.
- van der Aa LB, et al. Allergy 2011;66(2):170-7.
- Hougee S, et al. Int Arch Allergy Immunol 2010;151:107-117.
- Chichlowski M et al. JPGN 2012;55(3):321–332.
- Fukuda S, et al. Nature 2011;469:543–547.
- Huda MN, et al. Pediatrics 2014;134(2):e362–372.
- Wong CB et al. Nutrients. 2019 Aug; 11(8): 1724.
- Akiyama K, et al. Acta Neonatologica Japonica 1994;30, 130-137 (translated).
- Hattori K, et al. Japanese Journal of Allergology 2003;52:20-30.
- Sato Y, et al. Acta Neonatologica Japonica 2003;39:247.
- Patole S, et al. PLoS One 2014;9(3):e89511
- Patole SK, et al. J Matern Fetal Neonatal Med 2016;29(23):3751-5.
- Fukishama Laboratory Fukushi Japan 1992
Dette er en informationsside til sundhedsfagligt personale.
© 1996 – 2022 Nutricia